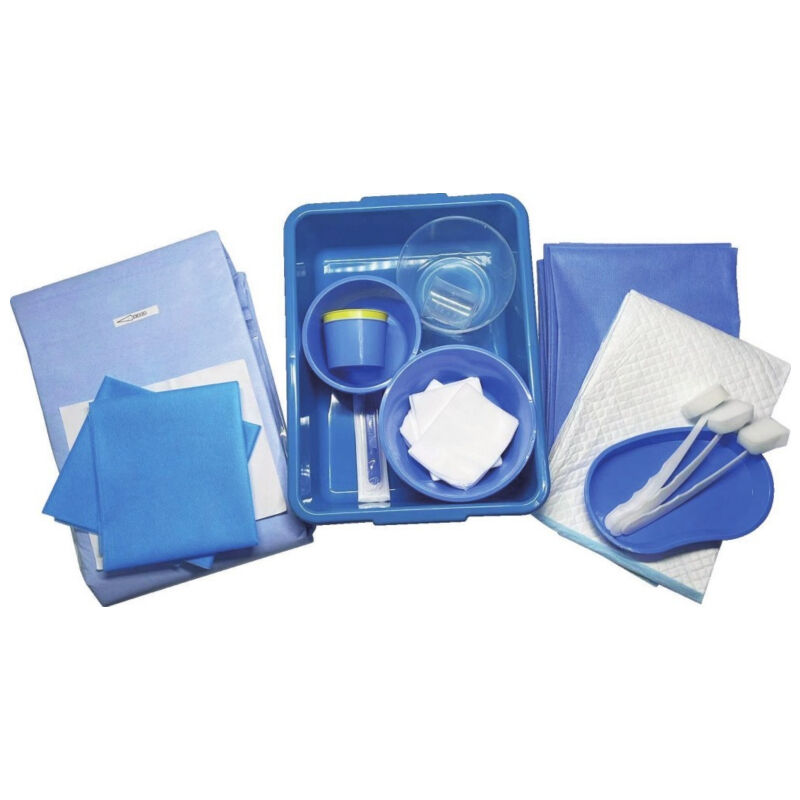
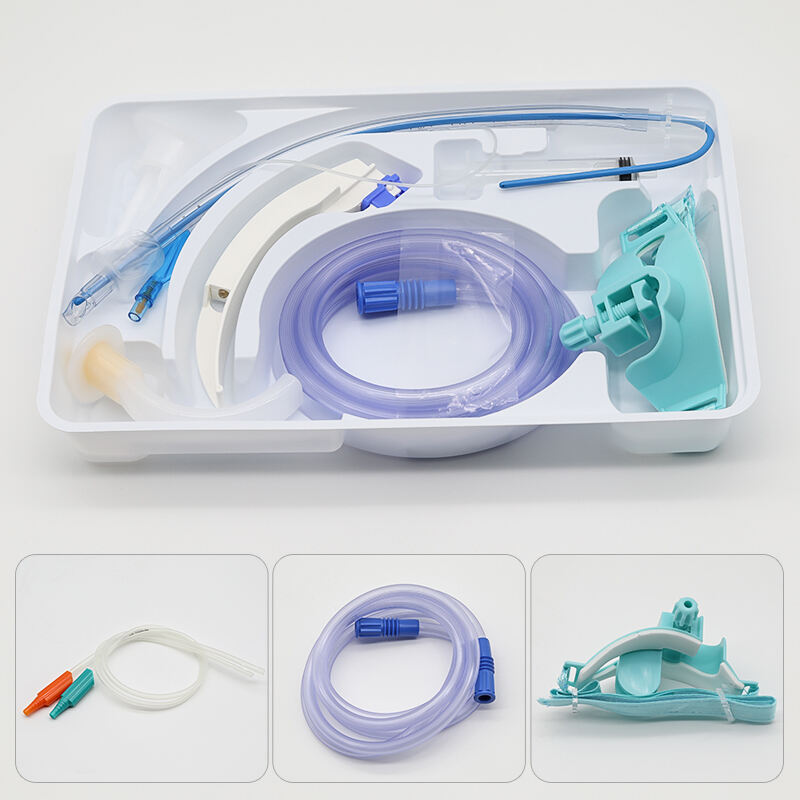
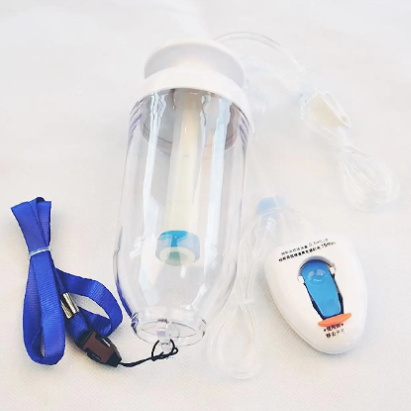
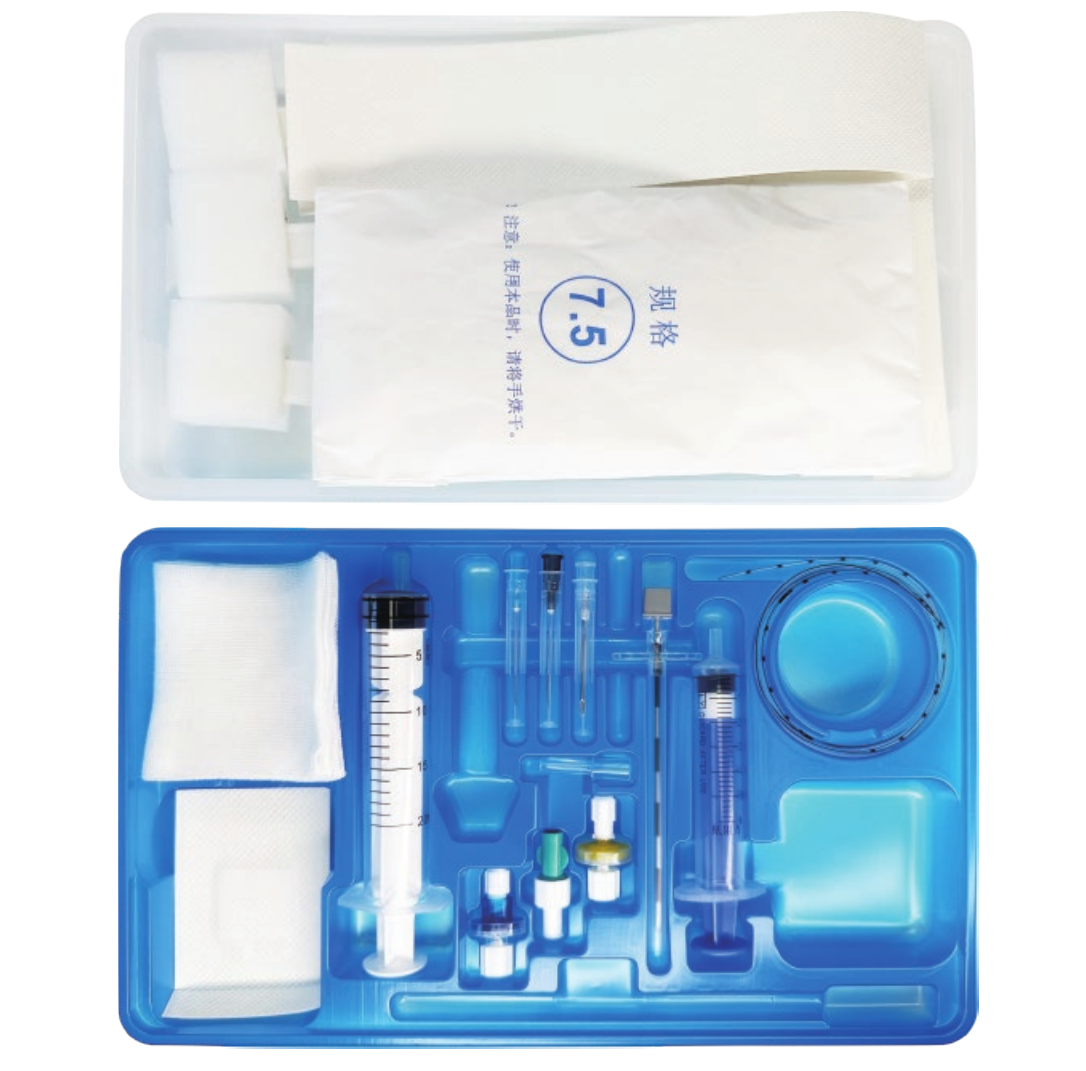
Reguleringsoverholdelse og kvalitetssikring på højt niveau
Prisen på epiduralkits omfatter omfattende reguleringsmæssige overholdelsesforanstaltninger og kvalitetssikringsprotokoller, der sikrer konsekvent ydelse og sikkerhed i alle medicinske anvendelser. Denne omfattende tilgang til overholdelse af regler repræsenterer en betydelig investering i produktionsprocesser, dokumentationssystemer og løbende overvågning af overholdelse, som beskytter sundhedsydelere og patienter samtidig med at opfylde de strengeste internationale standarder for medicinsk udstyr. FDA-godkendelsesprocesser for epiduralkits kræver omfattende kliniske tests, biokompatibilitetsstudier og langvarige sikkerhedsvurderinger, der strækker sig over flere år og indebærer betydelige finansielle investeringer fra producenterne. Prisen på epiduralkits afspejler disse omkostninger ved overholdelse af regler, mens den giver sundhedsfaciliteter tillid til, at deres medicinske udstyr opfylder eller overstiger alle relevante sikkerhedsstandarder. Internationale certificeringskrav, herunder CE-mærkning til europæiske markeder og godkendelser fra Health Canada, bidrager yderligere til det omfattende reguleringsramme, der understøtter produktion og distribution af epiduralkits. Kvalitetsstyringssystemer, der er implementeret af anerkendte producenter af epiduralkits, følger ISO 13485-standarder, der styrer kvalitetssystemer for medicinsk udstyr gennem hele produktets livscyklus. Disse systemer sikrer konsekvente produktionsprocesser, strenge testprotokoller og omfattende dokumentation, der understøtter sporbarhed og kvalitetsverifikation. Prisen på epiduralkits omfatter disse investeringer i kvalitetsstyring og leverer produkter, der demonstrerer konsekvente ydeevneegenskaber i store produktionsmængder. Partitestprocedurer bekræfter, at hver epiduralkit opfylder specifikationskravene gennem omfattende analyse af komponentmaterialer, dimensionel nøjagtighed og funktionalitet. Disse tests inkluderer steriliseringsvalidering, verifikation af emballagens integritet og bekræftelse af komponenternes kompatibilitet, hvilket sikrer, at alle kits, der leveres til sundhedsfaciliteter, opfylder høje kvalitetsstandarder. Certificering af produktionsfaciliteter kræver løbende inspektioner, validering af processer og initiativer til kontinuert forbedring, der opretholder de højeste niveauer af kvalitetssikring. Prisstrukturen for epiduralkits tager højde for disse facilitetsinvesteringer og de løbende omkostninger forbundet med at opretholde overholdelse af regler i flere jurisdiktioner. Efter-markeds-overvågningssystemer overvåger ydelsen af epiduralkits i kliniske indstillinger, hvor data indsamles om procedureresultater, uønskede hændelser og langvarige sikkerhedsprofiler, der informerer om løbende produktforbedringer. Denne overvågning udvider producentansvaret ud over den første salg for at omfatte løbende support til sundhedsydelere og patienter gennem hele produktets livscyklus. Prisen på epiduralkits omfatter disse forpligtelser efter salget og giver samtidig sundhedsfaciliteter adgang til producentens ekspertise og teknisk support, når det er nødvendigt. Dokumentations- og sporbarhedssystemer opretholder omfattende optegnelser over produktionsprocesser, kildehenvisning af komponenter og resultater af kvalitetskontrol, hvilket muliggør hurtig respons på eventuelle kvalitetsbekymringer eller reguleringsanmodninger.